Дрожжевые клетки перерабатывают сахар в этиловый спирт (этанол) в процессе двенадцати последовательных химических реакций, которые образуют реакционную цепь. Такой же путь — проходят до десятой ступени молочнокислые бактерии (те самые, что загрязняли чаны винодела Биго.)-; те же процессы происходят и в наших мышцах, когда им приходится делать внезапное усилие. Только на одиннадцатой ступени их путь разветвляется и становится иным, чем у дрожжей; при этом происходит превращение промежуточного продукта ^ (пировиноградной кислоты) в молочную кислоту вместо образования СО2 и этилового спирта.
Таким образом, спиртовое и молочнокислое брожение отличаются только в самом конце реакционной цепи. До этого они проходят один и тот же маршрут, известный как гликолитическая цепочка. Этот маршрут не оставляет заметного следа в цитозоле, ибо у «змеи» нет ощутимой плоти. Если мы оденем наши химические «очки», обладающие большим увеличением, то увидим хаотическое, беспорядочное движение молекул А, В, …, Л, К, смешанных с множеством других промежуточных продуктов других реакций. Объединяют все эти реакции и составляют плоть «змеи» стрелки; каждая из них указывает на наличие специфических ферментов (гл. 2), которые катализирурт указанные химические превращения. Последовательность участия двенадцати ферментов, вовлеченных в гликолитическую цепь, автоматически вытекает из природы их субстратов и продуктов реакций. Реакция, дающая начало образованию О из С, должна непременно последовать сразу же после превращения В в С и предшествовать образованию Е из Э. Для направления молекул к месту их назначения никаких физических каналов не требуется. Кажущийся хаос, который мы видим, заключает в себе высокую степень упорядоченности, динамическую организацию, обусловленную свойствами участвующих ферментов.
Этот урок гликолиза можно обобщить. За каждой из тысяч химических реакций, протекающих в живых клетках, скрывается фермент. Сейчас это общеизвестный факт, но его установили только после того, как была разгадана гликолитическая цепь, ответственная за спиртовое брожение в дрожжевых клетках. Энзимология, наука о ферментах, значительно обогатила наше понимание как самой жизни, так и химии и теперь начинает — приносить большую практическую пользу. Ферменты, выделенные из природных источников, широко используются в промышленности. Условия нашего путешествия не позволят нам детально останавливаться на этой важной отрасли биохимии. Но мы должны постоянно помнить о том, что любая наблюдаемая нами деятельность независимо от ее природы обусловлена каталитическим участием ферментов.
Ферментам, как правило, помогают до-полнительные вещества, называемые кофакторами или коферментами. В гликолизе необходимо обратить внимание на два кофактора. Один из них называется НАД, что означает никотинамидадениндинуклеотид. Как вы еще заметите, биохимики очень любят сокращения. Но у них есть оправдание: большинство веществ, с которыми им приходится иметь дело, слишком сложные, чтобы их можно было называть полностью при каждом упоминании. НАД — одно из них, и мы даже не будем пытаться рассматривать его химическую структуру. Однако хотелось бы отметить, что никотинамидная часть молекулы — это витамин РР, что означает pellagra preventiva. Его нехватка в пище вызывает пеллагру — тяжелое заболевание системы пищеварения, ранее широко распространенное на Американском континенте. И это не единственный пример. Большинство витаминов действуют как коферменты или являются их частью, именно поэтому ор-ж ганизм не может обходиться без витаминов. С функцией НАД мы познакомимся несколько позднее.
Другой кофактор, который следует рассмотреть, обозначается как АТФ, или аденозинтрифосфат. В конечном итоге нам придется изучать его структуру, но в данный момент необходимо знать лишь, что молекула АТФ может быть гидролизована (разрушена с помощью воды) на аденозиндифосфат (АДФ) и неорганический фосфат (Фн) и, наоборот, может быть образована (с потреблением энергии) при конденсации АДФ и Фн с выделением воды.Важность функции АТФ в процессе гликолиза выяснилась после того, как было показано, что разрушение глюкозы связано с образованием АТФ: при превращении каждой молекулы глюкозы в молочную кислоту или этиловый спирт происходило фосфорилирование двух молекул АДФ й превращение их в АТФ. Эта взаимосвязь непоколебима. Если синтез АТФ не происходит, например в случае нехватки АДФ, гликолиз прекращается.
Истинный смысл этого удивительного явления выяснился только после установления энергетики самого процесса. Брожение глюкозы приводит к высвобождению свободной энергии: на каждую грамм-молекулу (г-моль) распавшейся глюкозы образуется около 47 килокалорий (ккал). С другой стороны, образование АТФ из АДФ + Фн требует затрат энергии: около 14 ккал на 1 г-моль образующегося АТФ. Следовательно, из 47 ккал, высвобожденных при разрушении глюкозы, 2X14=28 ккал, или 60% идет на образование АТФ, вместо того чтобы рассеиваться в виде тепла. Гликолиз снабжает энергией синтез АТФ; в объединении этих двух процессов и заключается механизм восстановления энергии.
Изучение этого вопроса, как и прежде, началось с гликолиза. Когда позднее по-следовательно были открыты другие катаболические процессы, оказалось, что и они связаны с образованием АТФ. Не только гликолиз, но катаболизм в целом снабжает энергией процесс образования АТФ: взаимосвязь лежит в основе универсального механизма восстановления энергии.Что же можно сказать относительно самой молекулы АТФ? Зачем нужен ее синтез? Ответ на этот вопрос, вернее намек на ответ, впервые был получен в начале 1930-х годов, после того как выяснилось, что мышца, теряющая способность к гликолизу после отравления (моноиодуксусной кислотой), все же может осуществлять небольшую часть работы за счет запасенной, «связанной с фосфатом энергии». Со временем было показано, что химическая реакция, прямо связанная с сократи-тельным механизмом, есть не что иное, как гидролиз АТФ до АДФ и Фн. Следовательно, АТФ является недостающим связующим между гликолизом и мышечной работой. Гликолиз способствует образованию АТФ; расщепление АТФ снабжает энергией работу мышц.
Это было открытие необычайной важности, распахнувшее одну из главных дверей на пути к пониманию сущности живого. Ибо не только мышечная работа,но и практически любой другой вид работы, выполняемой живыми организмами, снабжается энергией от АТФ. Рассмотрим, хотя бы поверхностно, любой биодвигатель, будь то ионный насос в мембране, сократительные волокна в жгутике, генератор света в личинке светляка или любые другие сложные синтетические реакции, посредством которых живые организмы вырабатывают свои собственные компоненты: практически всюду мы обнаружим АТФ, выступающий в виде источника энергии. Это главное топливо жизни, и функция катаболизма заключается в способности поддерживать восстановление АТФ.
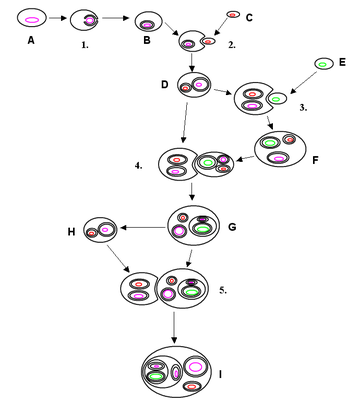
Иллюстрацией такого взаимодействия служит классический (исторический) пример анаэробных дрожжей. Этот организм растет и размножается, достигая удивительного совершенства химической инженерии и передачи информации, с тем только, чтобы могла образоваться одна — единственная новая крошечная клетка дрожжей, полностью похожая на свою предшественницу. Все это дрожжевая клетка делает за счет превращения сахара в спирт, используя этот процесс как единственный источник энергии. И эта энергия через АТФ питает тысячи различных процессов, подобно тому, как энергия сжигаемых угля или нефти, преобразованная в электричество, обеспечивает удивительные достижения современной технологии.