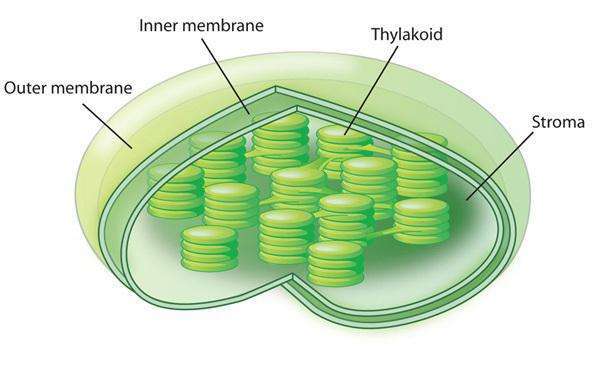
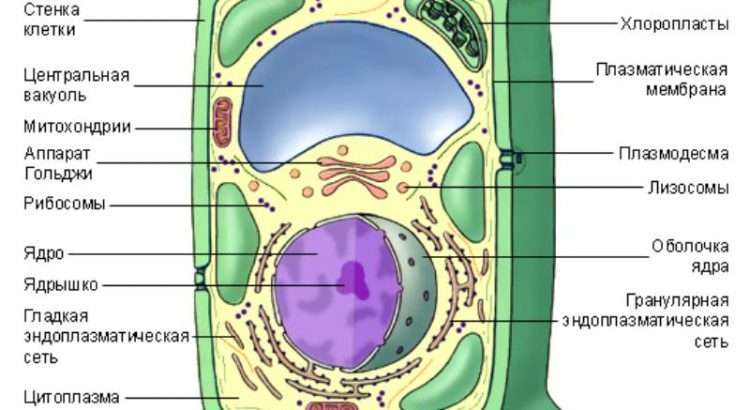
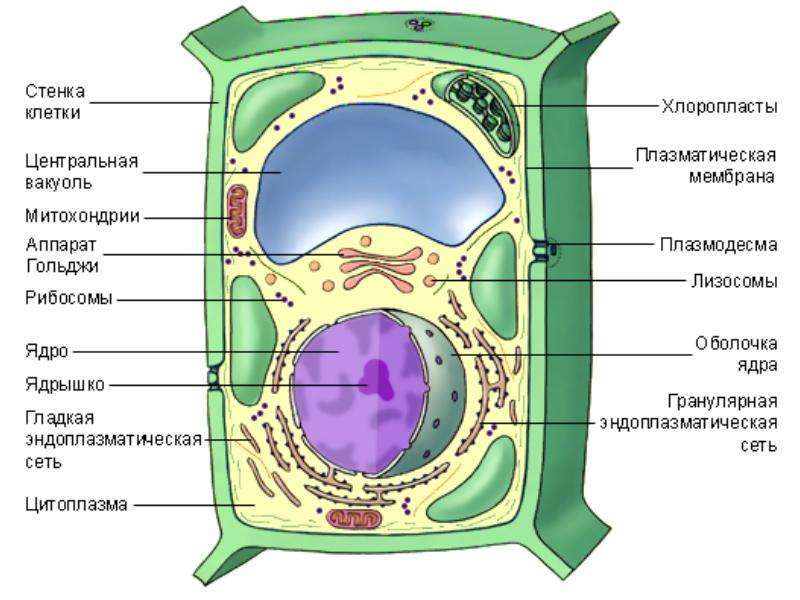
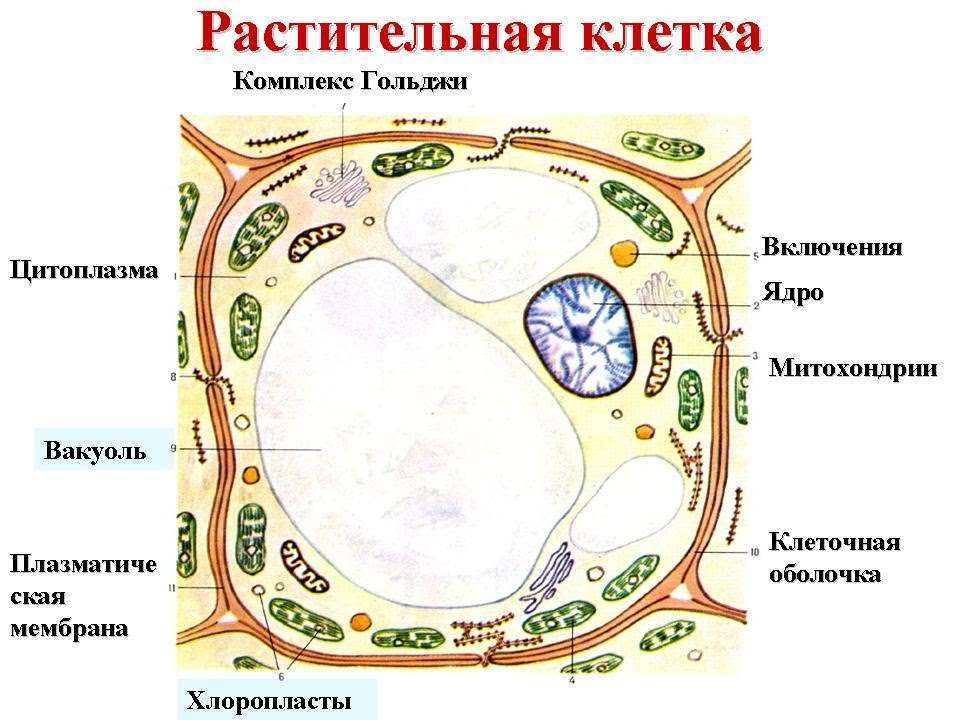
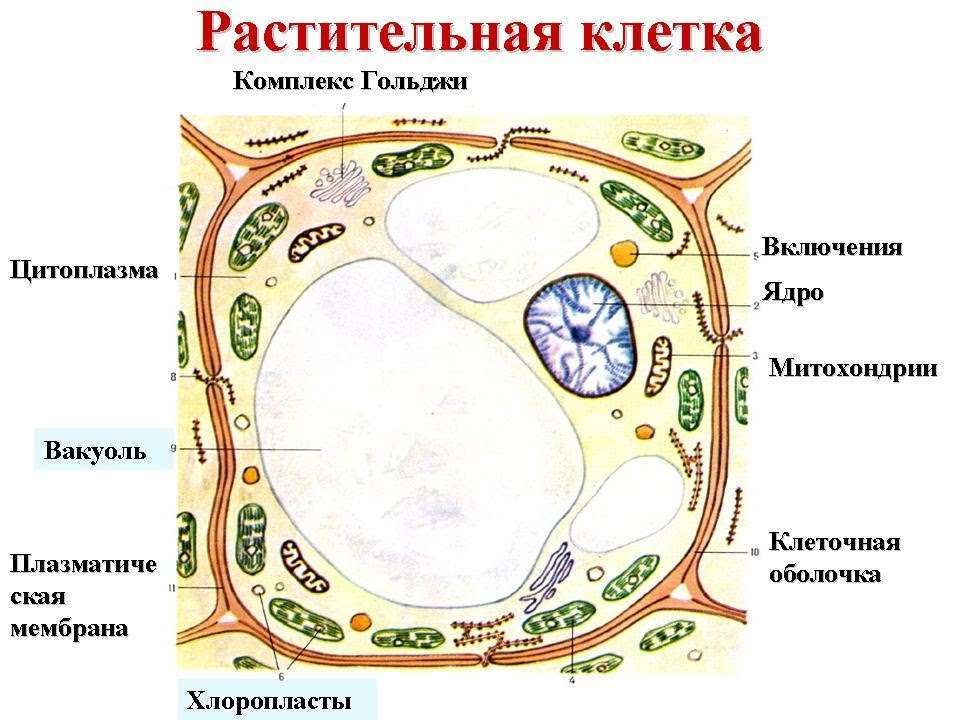
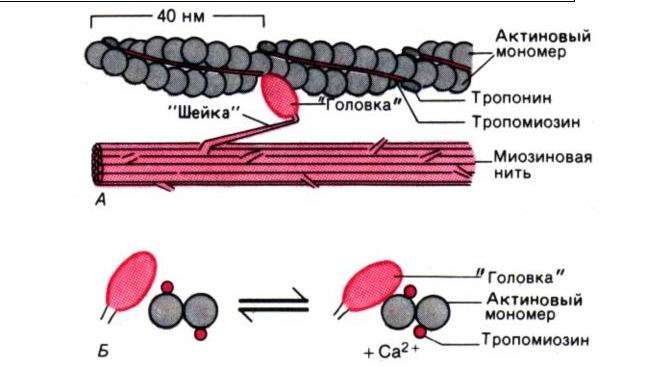
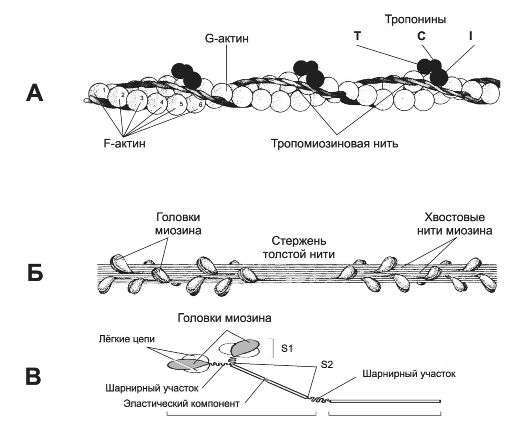
Хлоропласты напоминают митохондрии по наличию двух окружающих мембран: наружной, которая, как предполагают, произошла из системы вакуолей предковых фагоцитов, и внутренней, которая, по-видимому, унаследована от плазматической мембраны древних эндосимбионтов — сине- зеленых водорослей. Они отличаются от митохондрий размером и цветом. Как правило, они намного крупнее митохондрий. Их размеры достигают нескольких микрон, и нам в ходе нашего путешествия не составило бы особого труда проникнуть внутрь хлоропластов, не будь они переполнены множеством мембран.
Эти мембраны, как и митохондрии, произошли из складок внутренней мембраны, но с тем важным отличием, что выпячивания отделились от мембраны и образовали мешочки в форме дисков. Мешочки получили название тилакоидов. Несколько тилакоидов образуют цилиндрическую структуру, названную граной. Каждый хлоропаст состоит из нескольких гран, часто связанных трубчатыми соединениями. Система внутренних мембран поддерживает фотосинтетический аппарат.
Этот механизм включает фосфорилирующую электронно-транспортную цепочку, граничащую сбоку с двумя фотоэлектрическими единицами. Цепочка напоминает митохондриальные микросферы. Она также состоит из ряда структурно связанных электронных носителей, включающих металлопротеиды (железо, медь), флавопротеиды, хиноны и цитохромы. Электроны, циркулирующие через микросферы, подчиняются тем же ограничениям, что и в митохондриях; они выкачивают протоны наружу, создавая протонный потенциал. Но «наружу» в тилакоидах на самом деле означает «внутрь», так как тилакоид представляет собой запечатанный мешочек в отличие от митохондриальной кристы, которая является открытой внутренней складкой. В результате создается впечатление,будто митохондрии и хлоропласты накачивают протоны в противоположных направлениях. Однако это не совсем так. В каждой из этих структур отрицательно заряженная сторона мембраны ориентирована к матриксу.
Как и митохондриальная внутренняя мембрана, тилакоидная мембрана содержит АТФ-управляемый протонный насос, который находится в узелках, выступающих в пространство матрикса. Не совсем ясно, сколько последовательных окфос-блоков связано с электронно-транспортными цепочками. Установлено, что один, а возможно, два блока находятся на основном, нециклическом пути. Повидимому, на циклическом пути имеется дополнительный окфос-блок.
Сами фотосистемы состоят в основном из связанного с белком хлорофилла, с которым в свою очередь связаны различные количества второстепенных пигментов, таких, как красные или голубые фикобилины (тетрапирролы с открытыми концевыми группами, напоминающие пигменты желчи) и желтые, оранжевые или красные каротины и связанные с ними ксантофиллы . Когда листья начинают менять свой цвет, первым исчезает хлорофилл и ярким пламенем загораются второстепенные пигменты, радуя наш глаз осенним буйством.
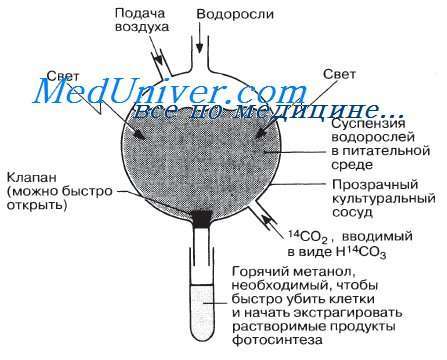
По определению вещество окрашивается в силу того, что поглощает какую-то часть падающего на него видимого света. Его цвет соответствует свету, который не поглощается, иными словами, дополняет поглощенный свет. Так, хлорофиллы зеленого цвета, так как они поглощают красный цвет (с длиной волны 680—700 нм); оранжевые каротиноиды поглощают голубой цвет (длина волны около 450 нм) и т. д.В тилакоидных мембранах имеется несколько сотен таких молекул, которые организованы в тесно связанные единицы, сгруппированные вокруг одной молекулы особого белково-хлорофиллового комплекса, обозначенного как Р 700 или Р 680 в фотосистемах I и II соответственно (в зависимости от длины волны максимального поглощения света). Чтобы лучше понять работу такой единицы, оставим ее на время в темноте, а затем внезапно осветим вспышкой света. Пигменты поглощают свет определенной длины волны (в зависимости от их спектра поглощения) и возбуждаются. Этот процесс включает дестабилизацию электрона внутри молекулярной структуры, что достигается количеством энергии, равным тому, которое соответствует поглощаемому кванту света.
У большинства пигментов энергия, полученная таким образом, быстро рассеивается в виде колебаний молекул (тепла) или иногда повторно излучается в виде света при более высокой длине волны (флуоресценция). При этом дестабилизированный электрон падает вниз до уровня, на котором он находится в состоянии покоя. Этого не происходит в Р-комплексах, что и определяет их биологическую эффективность. Благодаря своему стратегическому положению в тилакоидной мембране они переносят дестабилизированный электрон к акцептору более высокого электронного потенциала, расположенному поблизости, и заполняют образовавшуюся электронную пустоту (положительную ячейку) электроном, взятым от низкоэнергетического донора. Таким образом они способствуют подъему электрона с уровня донора на уровень акцептора с помощью световой энергии. В Р 680 донором является вода, а акцептором — носитель, расположенный где-то в верхней части электронно-транспортной цепи В Р 700 донором является цитохром, расположенный на выводной части электронно-транспортной цепи, а акцептором — ферредоксин — железосерный белок с высоким электронным потенциалом, который переносит электроны на НАДФ+ или в конечном счете вновь в электронно-транспортную цепь.
Вот почему пигменты Р представляют собой истинные фотоэлектрические преобразователи. Все дополнительные молекулы хлорофилла и других окрашенных веществ, с которыми они связаны в каждой фото синтетической ячейке, выступают только в роли коллекторов света или солнечных антенн. Их структура такова, что они способны обмениваться энергией друг с другом с исключительно высокой скоростью (возбужденный перенос), тем самым значительно повышая эффективность системы. Любой квант световой энергии, пойманный одним из компонентов ячейки, может быть доставлен к центральному пигменту Р и использован для фотоэлектрического преобразования. Это возможно при условии, что связанная с акцептором молекула свободна и в состоянии принять электрон, а кроме того, имеется донор, готовый заполнить освободившееся пространство.
Количество энергии, образующейся в результате улавливания кванта света, легко вычислить, пользуясь формулой Планка. Для красного цвета длина волны равна 700 нм, энергия — 6,77X Ю-20 кал/квант света, или 41 ккал/Э. Если один квант сдвигает один электрон через каждую фотосистему, что очень похоже на истину, потребуется 2X2X41 или 164 ккал световой энергии для того, чтобы перенести одну пару электрон-эквивалентов от воды к НАДФ+. Как мы уже видели, энергетический уровень в резервуаре НАДФН достигает примерно 55 ккал над уровнем вода/кислород. Таким образом, эффективность фотовосстановительного процесса порядка 34%. Но это справедливо лишь в том случае, если не принимать во внимание прироста АТФ. Перенос электронов от фотосистемы II к фотосистеме I происходит по меньшей мере через один окфос-блок, добавляя не меньше 8% к энергии, получаемой в виде АТФ. Что касается циклического фосфорилирования, осуществляемого через фотосистему I и электронно-транспортную цепь, ее минимальная эффективность составляет примерно 17%. Но эта минимальная величина может быть увеличена вдвое и даже втрое, если циркулирующие электроны проходят не через один, а через большее число окфос-блоков. Во-прос до конца не выяснен, как, впрочем, и многие тонкости на пути фотоэлектронов. Некоторые исследователи даже утверждают, что фотосистема II в состоянии сама поднимать электроны на всем пути от воды до НАДФ+; в данном случае эффективность процесса будет намного выше установленной нами ранее.
Даже самые низкие показатели работы этой системы при использовании одного кванта света намного выше, чем в фотохимических системах. Это необходимо иметь в виду тем, кто пытается приручить солнечную энергию. Превзойти многоклеточное покрывало, состоящее из бесчисленного множества микропреобразователей, которые цианобактерии и их потомки сплели вокруг Земли, — задача не из легких. Быть может, стоит попытаться найти более эффективные пути, чтобы заставить эти организмы работать на нас, а не соперничать с ними.