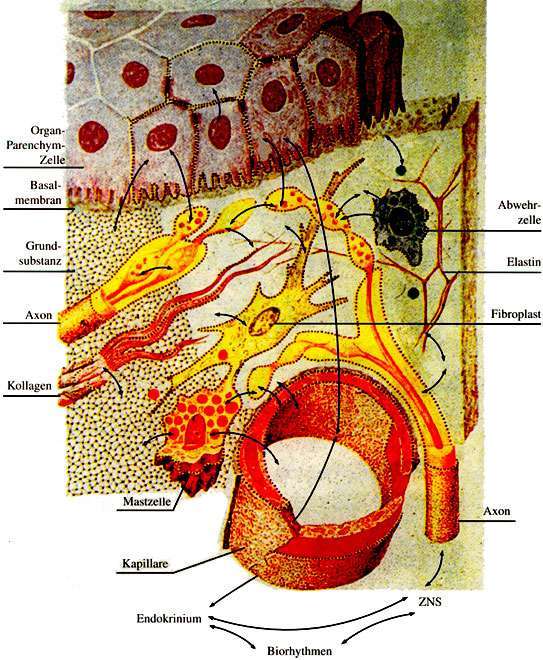
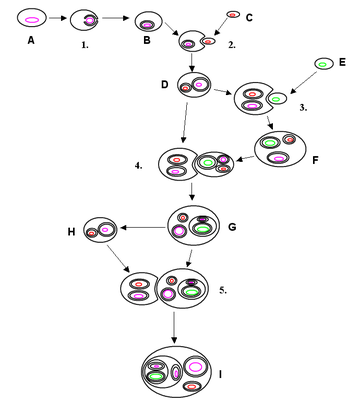
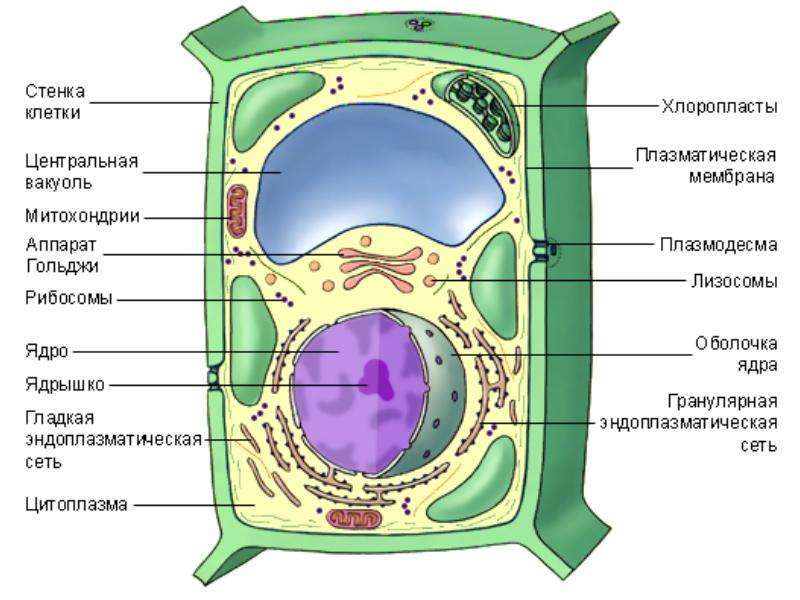
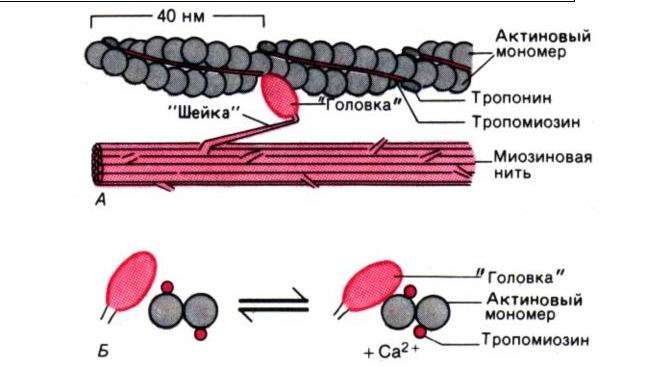
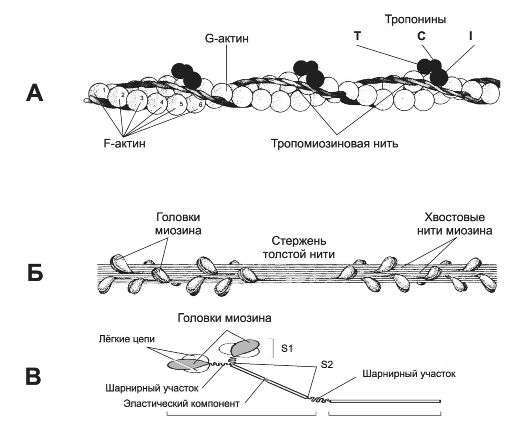
Митохондриальные энергетические преобразователи располагаются исключительно внутри розового, складчатого «футляра», который образует внутреннюю мембрану телец. Это очень тонкая оболочка толщиной 7 при нашем увеличении в миллион раз она составит чуть больше 60 мм. Снаружи она гладкая, а изнутри покрыта мелкими узелками. Узелки имеют в диаметре около 9 им (что составляет примерно 80 мм при увеличении в миллион раз) и прикрепляются к мембране короткими, узкими стволиками, отчего внутренняя сторона мембраны похожа на поверхность, покрытую крошечными грибами.Для дальнейшего исследования нам потребуется наше молекулярное увеличительное стекло. Вид, который открывается с его помощью, поистине удивителен; это один из величайших шедевров молекулярной инженерии. Вся поверхность мембраны покрыта микросферами; каждая из них состоит из 15—20 различных видов электронных носителей, объединенных для обеспечения необходимого электронного переноса. В одном-единственном теле митохондрий может существовать почти 100 000 таких микросфер.
Эти микросферы, обычно называемые дыхательными цепочками, включают набор различных молекул. Наиболее известные среди них — флавины и гемы. Флавины — удивительный класс зеленовато-желтых пигментов, образованных из рибофлавина, или витамина Вг. Наиболее важными флавиновыми производными являются флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). Их основное свойство заключается в способности выступать в роли носителей водорода. Таким образом, они служат коферментами для многочисленных фла — виновых дегидрогеназ.
Гемы близкие родственники хлорофиллов, зеленых фотосинтетических пигментов, с которыми их роднит одно характерное свойство: наличие порфиринового ядра — плоской, дискообразной молекулы, состоящей из четырех пиррольных колец, связанных метеновыми (—СН=) мостиками. В центре диска имеется отверстие, окруженное электронами четырех резонирующих атомов азота. Если мы поместим в отверстие ион магния, то получим молекулу хлорофилла. При замене иона магния на ион железа получится гем Благодаря свойству железа принимать форму двухвалентного (Ре2+) или трехвалентного (Ре3+) иона гем представляет собой электронный носитель:
Гем—Ре2+ ^ Гем—Ре3+ + е~.
В комбинации с белками гемы образуют целый набор «доспехов», состоящий из разноцветных молекул с оттенками от кроваво-красного до горохово-зеленого. Все они в той или иной степени участвуют в утилизации кислорода. Наиболее известная функция заключается в доставке кислоро-да, который переносится красным кровяным пигментом — гемоглобином. В дыхательной цепочке гемопротеиды представлены рядом цитохромов, названных так из-за того, что они были обнаружены среди самых первых пигментов, постоянно присутствующих в клетках.
Помимо двух упомянутых главных классов переносчиков электронов дыхательная цепь содержит дифенолы, которые окисляются до соответствующих хинонов,железосерные белки, в которых ионы, несущие электроны, заключены в оболочке сульфгидрильных групп, связанные с белками ионы меди и, возможно, другие компоненты. Отметим (как тему для дальнейшего обсуждения), что одни из этих молекул выступают непосредственно как электронные носители (гемопротеиды и металлопротеиды), тогда как другие переносят атомы водорода (т. е. электроны в комбинации с протонами).
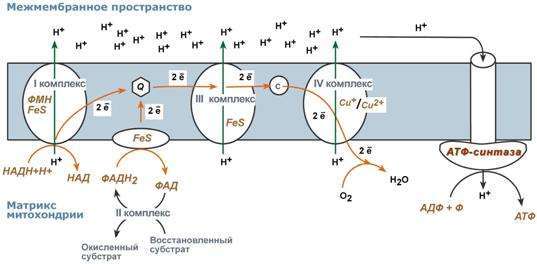
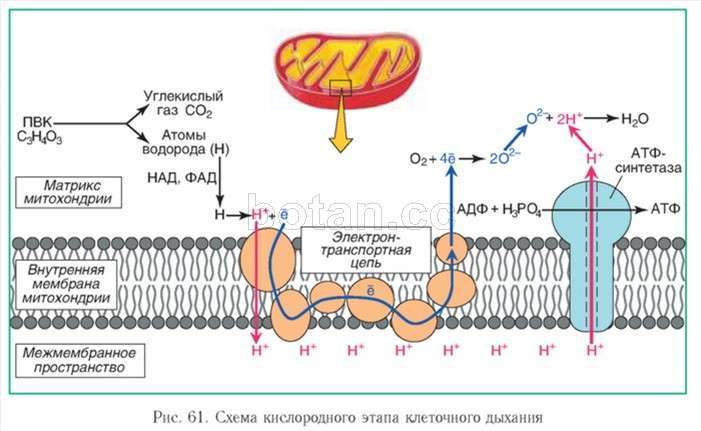
Внутри каждой дыхательной микросферы эти различные молекулы организованы таким образом, что могут работать как высокоэффективные «сборочные бригады» электронов. Это означает прежде всего, что они построены в виде нисходящих электронных потенциалов, поэтому электроны могут легко падать от одного компонента к другому. Кроме того, они ориентированы друг к другу так, чтобы их активные центры могли легко обмениваться электронами с партнерами по обеим сторонам; для достижения необходимых контактов достаточно только малейших изменений положения, вызванных тепловыми колебаниями и вращениями. И наконец, они должны подходить к соответствующим входным и выходным отверстиям. Как мы увидим, главный вход обеспечивается флавопротеидным ферментом, который переносит электроны от матричной НАДН к верхней части дыхательной цепи. На более низких энергетических уровнях существуют несколько вторичных вводов. Главное выводное отверстие ведет к кислороду через сложный комплекс цитохромов и меди, известный в настоящее время как цитохромоксидазы, но первоначально названный его первооткрывателем, немецким биохимиком Ото Варбургом, дыхательный фермент. Нам это название представляется наиболее подходящим, поскольку большая часть кислорода, потребляемого для дыхания, в биосфере ис-пользуется благодаря данному ферменту.
Для сборки такой электронно-транспортной цепи требуется большое искусство. И все же эти архитектурные ухищрения кажутся почти тривиальными по сравнению с некоторыми другими свойствами дыхательной цепи, так как микросферы являются не только электронными проводниками. Они также проводники энергии, организованные таким образом, чтобы улавливать энергию, излучаемую электронами по мере их падения к кислороду, и тем самым подготовить их к использованию в биологической работе с АТФ. Другими словами, в микросферах содержатся окфос-блоки.
Это вносит два дополнительных условия в их устройство. Во-первых, потенциал носителей должен быть сбалансирован таким образом, чтобы обеспечить необходимое падение электронов. Вспомним: для производства парой электронов энергии, достаточной для поддержания синтеза молекул АТФ, электроны должны упасть вниз с разностью потенциалов как минимум 300 мВ. Во-вторых, электроны, претерпевающие такие падения, должны подчиняться условиям, так или иначе связывающим их поток с синтезом АТФ. Такая же картина наблюдается при прохождении потока воды через гидротурбину, в результате чего вырабатывается электричество.
Первое условие обеспечивается весьма умело и эффективно. На пути движения электронов имеется по крайней мере три окфос-блока или фосфорилирующих участка, объединенных вместе. Это так называемые участки I, II и III, разделенные плат формами, которые мы обозначим как уровни НАДН, Ь — Начнем с рассмотрения уровня с. Он получил название от цитохрома с, своего основного компонента. Среди веществ, способных отдавать электроны в цепь на этом уровне, имеется аскорбиновая кислота, или витамин С—’вещество, содержащееся в свежих фруктах и овощах и пред-отвращающее развитие цинги — обычной болезни мореплавателей в прошлом. (Слово «аскорбиновая» произошло от сочетания греческой приставки «а», означающей «нет», и английского слова зсогЬи! — цинга.) Не ясно, связано ли противоцинготное свойство витамина С непосредственно с его способностью отдавать электроны, хотя и не исключено, что это осуществляется каким-то особым путем. Однако в лабораторных экспериментах аскорбиновая кослота взаимодействует с митохондриями на с-уровне, и это позволило выявить окфос-блок на участке III, когда обнаружилось, что одна молекула АТФ синтезируется для каждой пары электронов, перенесенной с аскорбиновой кислоты на кислород
Подход к участку II осуществляется через Ь — Q-уровень, названный так потому, что в нем находятся одновременно цитохром Ь и кофермент С, или убихинон — электронный носитель хинонового типа. С уровнем Ь — С? связано несколько ФАД-зависимых флавопротеидов: они служат входными отверстиями для электронов, поступающих от определенных метаболических субстратов, таких, как янтарная кислота — промежуточный продукт цикла Кребса и жирные производные ацилкофермента А — активированные формы жирных кислот. Когда пара электронов поступает на этот уровень, она падает вниз через два последовательных окфос-блока. При этом образуются две молекулы АТФ.
Уровень НАДН занят специфическим флавопротеидом, который переносит электроны от НАДН на участок I фосфорилирования. Для каждой электронной пары, поступающей на этот уровень и собираемой кислородом на дне, синтезируется всего три молекулы АТФ. НАД+ сам по себе служит электронным акцептором в бесчисленном ряде реакций. Таким образом, в этот поток направляется большинство катаболических электронов у аэробных организмов.
Эффективность этих митохондриальных трансформаторов поистине удивительна. При участии НАДН, выступающего в роли донора электронов, свыше 85% свободной энергии окисления восстанавливается в виде АТФ: ЗХ 14=42 ккал на пару электрон — эквивалентов из общей суммы 49. При участии ФАДН2 эффективность ‘ несколько меньше, но все же значительна и составляет 2X14=28 ккал на пару электрон-эквивалентов из 37, или 76%.
В сочетании с высокой эффективностью реакций холодного сгорания общая эффективность процесса достигает 80%. Эту величину легко рассчитать по данным, приведенным в табл. 4. А данные эти просто ошеломляют! С ними не идут в сравнение никакие источники энергии, созданные руками человека. Они отражают удивительное свойство энергетических преобразователей, заключенных в микросферах внутренней мембраны митохондрий.
Механизм работы этих преобразователей занимал умы лучших исследователей более трех десятков лет. По мнению английского ученого Питера Митчелла, родоначальника широко распространенной хемиосмотической теории, все дело в движущей протоны силе. Эта проблема для туристов представляет исключительную трудность, но все же попытаемся к ней приблизиться. Ибо, как нам станет ясно из гл. 10, это один из центральных механизмов жизни, а потому его рассмотрение стоит затраты дополнительных усилий.